L’utilisation d’antioxydants en élevage est destinée à contrecarrer les conséquences délétères des radicaux libres issus de l’alimentation ou du métabolisme sur la santé et la performance. Prendre les précautions d’usage en vue de diminuer les risques (aliment avec moins de lipides insaturés par exemple) ne suffira pas à éviter totalement le stress oxydatif. Les acides gras insaturés ont des vertus, les animaux d’élevage un métabolisme très élevé et producteurs de radicaux libres. Il faudra donc utiliser des antioxydants.

Se pose alors la question du choix : pourquoi préférer un antioxydant plutôt qu’un autre ? Nous ne traiterons pas ici de la stratégie de protection des aliments en complément de celle des animaux. La question qui reste est celle de la comparaison de l’efficacité d’un produit plutôt que d’un autre sur une application donnée.
Antioxydants : Les différentes méthodes analytiques d’estimation de l’efficacité
Un des critères mis en avant par les fabricants d’additifs destinés à l’alimentation animale est l’efficacité comparée de leur produit versus la vitamine E. Mais chacun y va de sa méthode. Si la méthode ORAC semble faire référence, elle n’est pas non plus toujours utilisée de la même manière.
2 grandes familles de méthode analytique disponibles
Toutes les méthodes d’analyse du pouvoir « antioxydant » d’un produit sont basées sur une réaction d’oxydo-réduction in vitro.
Exemple de réaction, l’oxydation de l’H2 par la fluorine : H2 + F2 → 2 HF
Il s’agit toujours de mesurer directement ou indirectement la disparition ou l’apparition d’un des composés de la réaction. Il existe 2 grandes familles de classification du pouvoir antioxydant d’un produit :
- les méthodes basées sur un transfert d’électron : Folin, TEAC
- les méthodes basées sur un transfert d’H : ORAC, Photochem
Quelle famille peut-on retenir ?
Les méthodes basées sur le transfert d’électrons ne tiennent pas compte du nombre d’électron qu’un antioxydant peut fournir. Leurs résultats sont donc peu fiables pour comparer 2 produits entre eux. Elles restent toutefois utiles pour un contrôle qualité d’un produit donnée afin de vérifier sa conformité avec ses spécifications.
Les méthodes basées sur le transfert d’hydrogène sont certes plus fiables mais restent théoriques car le produit testé est toujours en excès pour que la réaction chimique soit aussi complète que possible. Cette situation est loin d’être représentative de ce qui se passe in vivo.
La méthode Photochem utilise la disparition d’un radical très présent dans les cellules : l’O2–. La méthode ORAC utilise elle un dosage indirect d’un radical de synthèse. Cette méthode est donc moins directe et moins représentative du métabolisme
De l’importance des solvants utilisés
La méthode ORAC est la plus reconnue. Pourtant, cette méthode présente de nombreuses variantes qui perturbent un peu le jeu. En effet le produit doit être solubilisé, pour cela la méthode ORAC propose une variante pour produits hydro-solubles et une variante pour produits liposolubles. Pour les liposolubles, on trouve autant de variantes que de solvants adaptés. Si le TROLOX (Vitamine E hydrosoluble) est toujours la référence, le choix du solvant influence grandement le résultat obtenu.
La méthode Photochem fait beaucoup moins référence que l’ORAC. En revanche elle est ouverte à plus de type de solvants comme les alcools par exemple. Mais si cette méthode permet de travailler avec un plus large spectre d’antioxydants, l’effet solvant reste un biais et interdit là aussi toutes comparaisons.
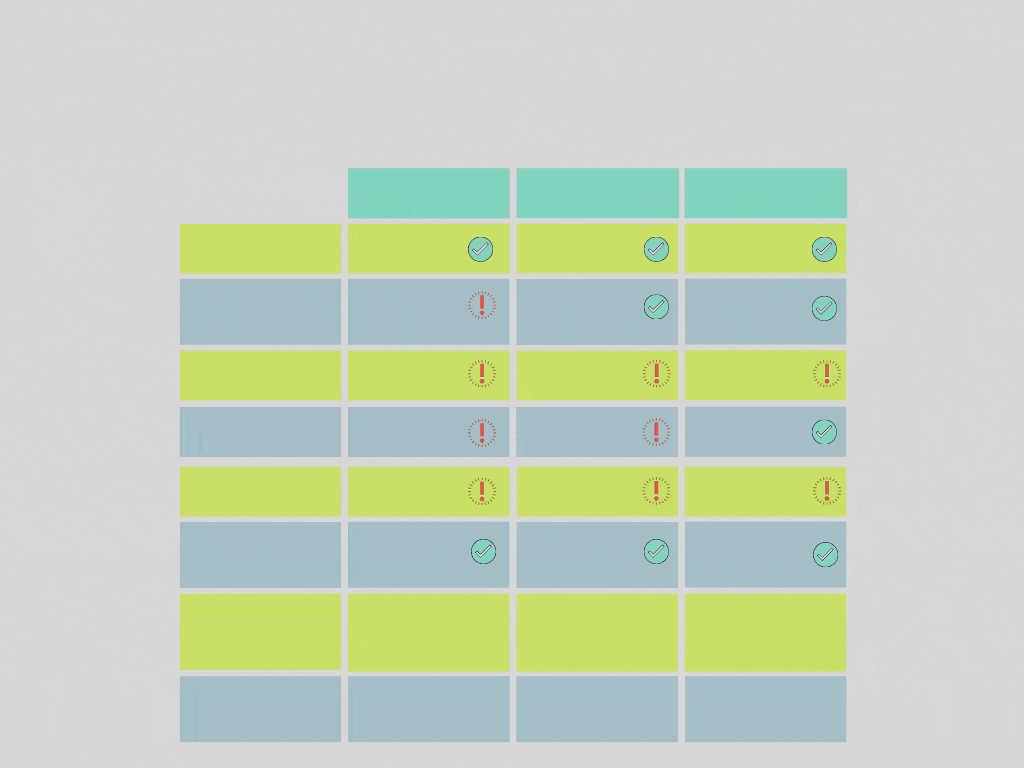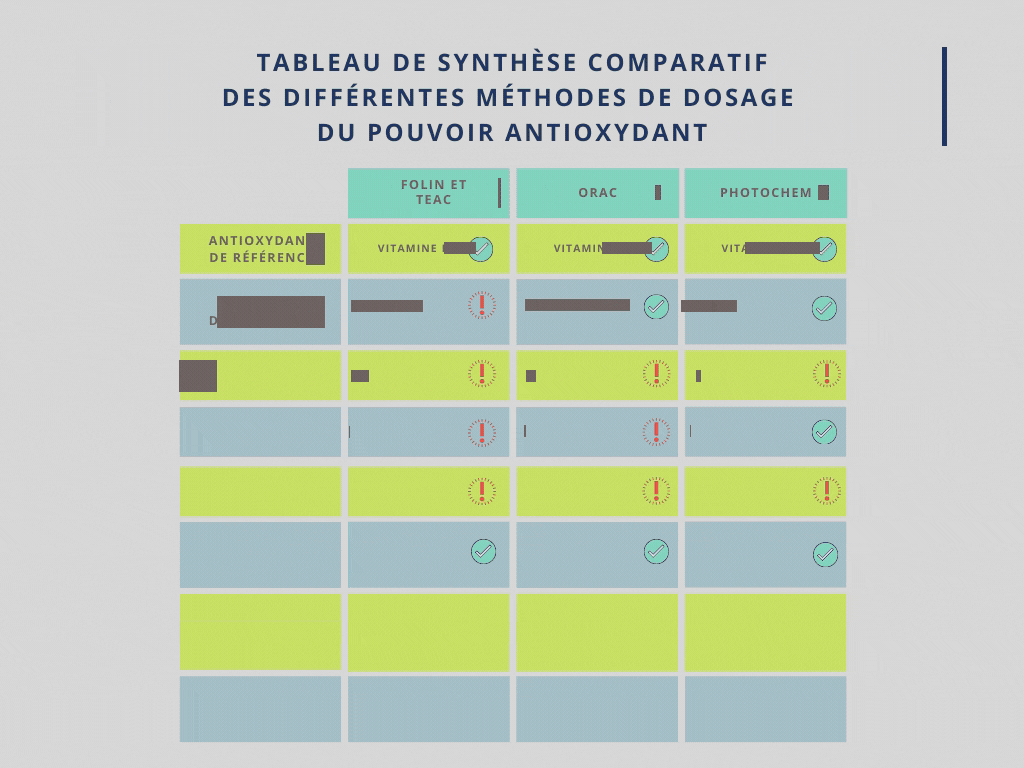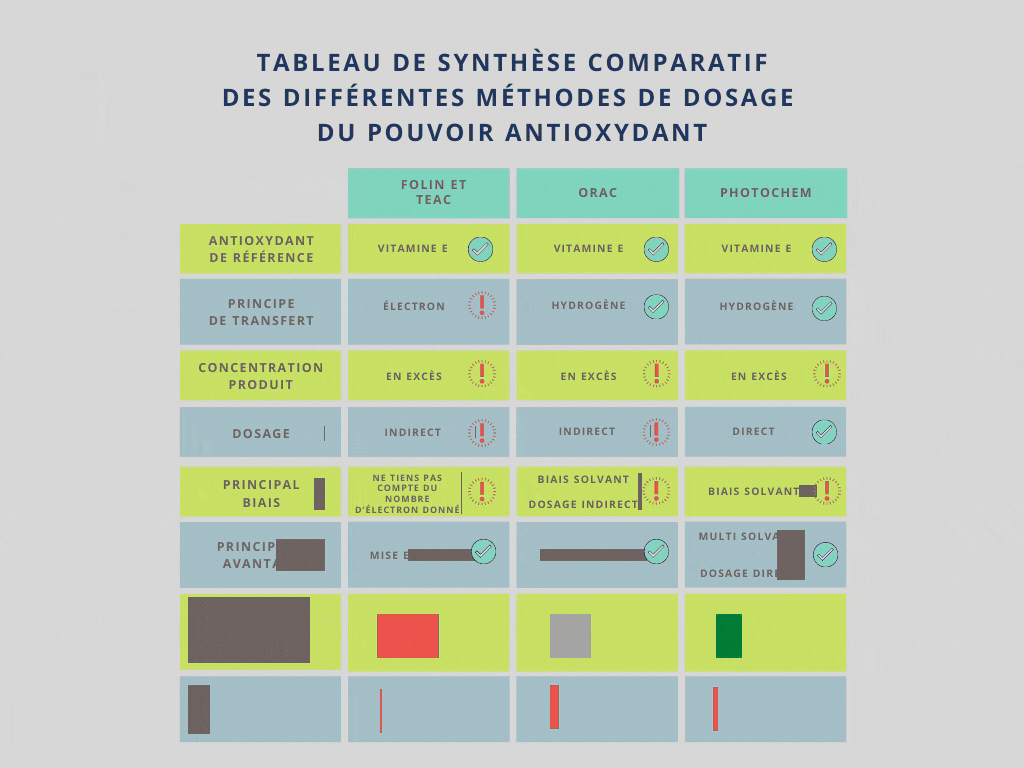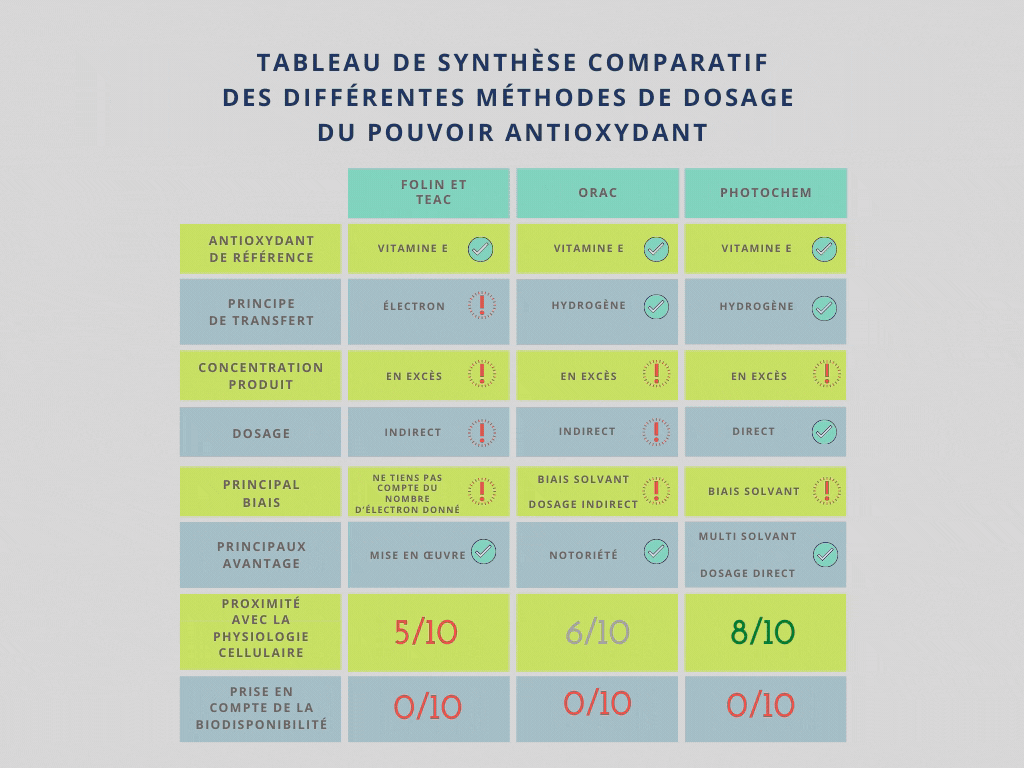
Tableau de synthèse comparatif des différentes méthodes de dosage du pouvoir antioxydant
Comment comparer des résultats obtenus avec des méthodes différentes ?
Afin de pouvoir comparer tous ces produits sur un même pied d’égalité, certains auteurs proposent de tout rapporter en équivalent TROLOX ou équivalent vitamine E. En effet, toutes ces méthodes ont pour point commun de comparer la capacité d’un antioxydant par rapport à celle du TROLOX. Ceci n’est absolument pas possible car d’une méthode à l’autre mais aussi d’un solvant à l’autre, les ratios entre antioxydants et vitamine E changent. Il est donc illusoire de les comparer dans l’absolu. Ces méthodes ne sont pas faites pour cela.
Des méthodes analytiques pour vérifier la conformité produit
En revanche, ces méthodes restent particulièrement utiles pour vérifier qu’un produit est conforme à ses spécifications par rapport à une méthode donnée. En effet, les antioxydants sont par nature instables et se dégradent dans le temps. La détermination de leur DLUO, de leur qualité doit être suivis par un plan de contrôle strict. Dans ce cas, on utilisera toujours le même protocole et les résultats seront comparables.
Et le mode d’action des antioxydants dans tout ça ?
D’ailleurs si nous avons besoins de plusieurs méthodes différentes pour mesurer le pouvoir antioxydant de différents produits, c’est aussi car leur mode d’action et les milieux dans lesquels ils vont agir sont différents. C’est pourquoi il vaut mieux rechercher une complémentarité, à minima un ciblage du produit sur la problématique de l’animal. Préférez par exemple un antioxydant à base de curcumine pour une problématique ayant des répercussions inflammatoires ou plutôt des procyanidines de raisin pour réduire des radicaux libres intestinaux. Finalement, seul l’animal peut nous indiquer quelle est la dose efficace pour un problème donné.
Conclusion
Toutes ces méthodes in vitro ont des qualités variables mais les mêmes défauts :
- L’antioxydant testé est en excédent pour le bon déroulement de la réaction redox alors que dans la nature, c’est le contraire
- Aucune de ces méthodes ne peut prendre en compte la biodisponibilité d’un actif
La meilleure méthode reste donc de demander à l’animal ce qu’il en pense. Des tests in vivo avec paramètre sanguin du statut oxydatif corrélés avec de bons indicateurs de production resteront toujours les seuls juges de paix.